- Imprimer
- Partager
- Partager sur Facebook
- Partager sur LinkedIn

Contexte
Avec plus de 537 millions de malades dans le monde actuellement, et plus de 783 millions d’ici 2045, le diabète est un problème de santé publique [GBD Diabetes Coll, 2023]. C’est une maladie chronique diagnostiquée par une glycémie à jeun ≥ 1,26 g/l qui apparaît lorsque le pancréas ne produit plus suffisamment d’insuline et/ou que l’organisme ne répond plus correctement à l’insuline qu’il produit (insulino-résistance ou IR). On distingue essentiellement 2 types de diabète : le diabète de type 1 (DT1) qui est une maladie auto-immune survenant chez l’enfant ou les jeunes adultes et aboutissant à une destruction progressive des cellules β pancréatiques, et le diabète de type 2 (DT2) survenant chez l'adulte présentant, dans 80% des cas, une surcharge pondérale voire une obésité.
Parallèlement à l’IR, l’obésité est associée à une réponse inflammatoire chronique, caractérisée par une production anormale de cytokines produites par le tissu adipeux et par l’activation de voies de signalisation pro-inflammatoires. Cette association n’est pas fortuite, et il a été montré dans plusieurs modèles animaux que ces phénomènes inflammatoires sont liés de façon causale à l’obésité et à ses comorbidités : IR, DT2 et l’athérosclérose.
Projets
La thématique maladies métaboliques comprend actuellement trois grands projets.
Imagerie moléculaire des cellules β pancréatiques
Développement de nouveaux radiotraceurs pour l’évaluation de la masse fonctionnelle des cellules β pancréatiques par imagerie nucléaire
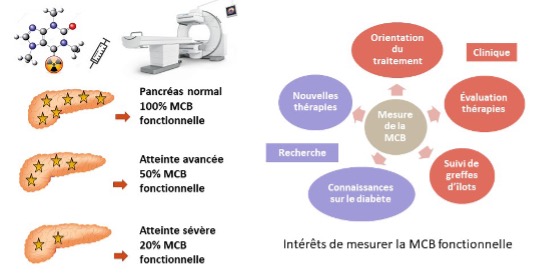
La fonction essentielle des cellules β pancréatiques est la sécrétion d'insuline en réponse à une augmentation de la glycémie. Ces cellules sont regroupées dans de petites structures de 50 à 300 µm de diamètre, les îlots de Langerhans qui ne représentent que 1 à 2% de la masse du pancréas et qui sont largement dispersés dans le pancréas exocrine. La diminution de la masse anatomique et/ou fonctionnelle des cellules β pancréatiques (MCB) est une caractéristique commune au DT1 et au DT2. Pouvoir estimer la MCB in vivo permettrait au clinicien d’évaluer et de suivre l’état anatomique et fonctionnel du pancréas d’un patient donné et ainsi d’orienter son traitement. Par ailleurs, les progrès réalisés dans les techniques de greffe de cellules β pour traiter les patients atteints d'un diabète de type 1 rendent le développement d'un outil permettant d'évaluer cette fonctionnalité après une greffe de plus en plus essentiel. En recherche, une telle modalité d'imagerie permettrait également l'évaluation de nouveaux traitements. De nombreuses techniques ont été proposées, en particulier l'IRM, la TEP (Tomographie par Émission de Positons) ou la TEMP (Tomographie d'Emission Mono Photonique), mais les résultats sont le plus souvent obtenus in vitro ou ex vivo et à l'heure actuelle, aucune n’est disponible en clinique.
Ce projet concerne la mise au point d'un nouveau traceur, utilisable en médecine nucléaire de façon routinière, spécifique des cellules β et capable via l'imagerie nucléaire d'estimer la masse fonctionnelle de ces cellules in vivo.
Imagerie de l’inflammation dans la MASLD
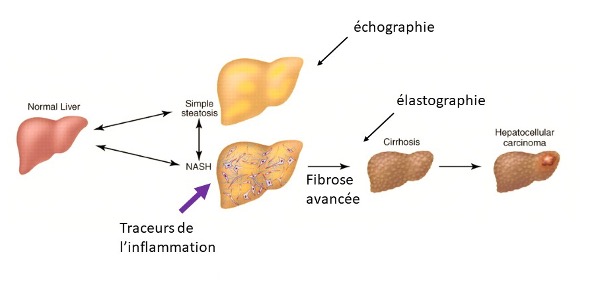
La MASLD (Metabolic dysfunction-Associated Steatotic Liver Disease) est généralement asymptomatique, au moins jusqu’aux stades avancés. Par conséquent, les patients progressent silencieusement et développent finalement une cirrhose et/ou un carcinome hépatocellulaire. Elle est caractérisée par la présence excessive de lipides hépatiques et inclut un large spectre d’atteintes hépatiques allant de la stéatose simple à la stéatohépatite (ou MASH) qui affecte environ un tiers des patients avec une MASLD. Au contraire de la stéatose simple, la MASH est associée à long terme à un mauvais pronostic, à une fibrose progressive, ainsi qu’un risque cardiovasculaire plus élevé. C’est un véritable problème de santé publique étroitement lié à l'obésité. Malgré sa prévalence croissante, aucun diagnostic non invasif n’est disponible pour les phases précoces de la pathologie et aucun traitement n’est efficace.
L’objectif de ce projet est de valider et proposer une méthode d’imagerie nucléaire non invasive des marqueurs précoces de la maladie, en particulier l’inflammation.
Imagerie moléculaire de la sénescence cellulaire
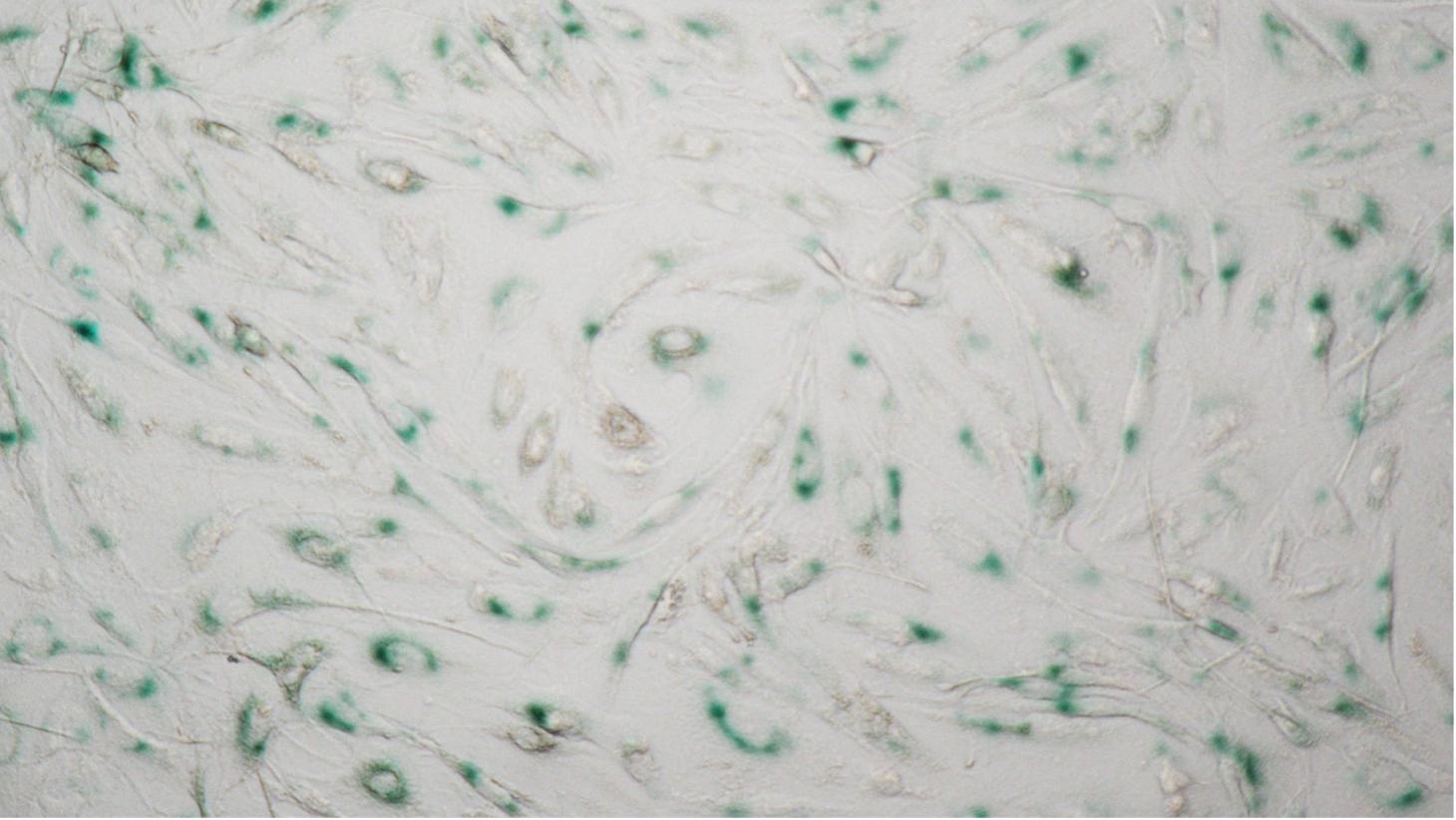
La sénescence cellulaire est un état permanent d'arrêt du cycle cellulaire, associé à une dérégulation métabolique, à diverses altérations macromoléculaires, et à l'acquisition d'un phénotype sécrétoire pro-inflammatoire. Ces changements peuvent entraîner une perte de fonction tissulaire. Les cellules sénescentes jouent un rôle dans de nombreuses pathologies chroniques, notamment les maladies métaboliques du foie et l'insuffisance cardiaque.
Les sénothérapies, traitements ciblant spécifiquement ces cellules sénescentes, représentent une stratégie thérapeutique innovante avec un large éventail d'applications potentielles dans le contexte du vieillissement et des maladies chroniques. Cependant, une des difficultés dans l'évaluation de ces agents, et à plus long terme dans l'évaluation de la réponse à ces traitements, est l'absence de méthode fiable pour détecter et quantifier la charge en cellules sénescentes in vivo.
Dans ce contexte, un projet mené au sein du LRB vise à développer un agent d'imagerie moléculaire permettant de visualiser la charge en cellules sénescentes de manière non invasive.
Valorisation
Nachit M, Montemagno C, Clerc R, Ahmadi M, Briand F, Bacot S, Devoogdt N, Serdjebi C, Ghezzi C, Sulpice T, Broisat A, Leclercq IA, Perret P. Molecular imaging of liver inflammation using an anti-VCAM-1 nanobody. Nat Commun 14(1):1062, 2023. https://www.nature.com/articles/s41467-023-36776-7
La société Hepavue Dx a été fondée pour exploiter l'utilisation du nanobody cAbVCAM1-5 dans la MASLD et un contrat de licence lui a été octroyé par l’UGA (Université Grenoble Alpes) et la VUB (Vrije Universiteit Brussel) pour cette seule indication.
Contact
Responsables
Cellules beta :
Pascale Perret
pascale.perret univ-grenoble-alpes.fr (pascale[dot]perret[at]univ-grenoble-alpes[dot]fr)
univ-grenoble-alpes.fr (pascale[dot]perret[at]univ-grenoble-alpes[dot]fr)
Tél +33 (0)4 76 63 71 02
MAFLD :
Pascale Perret
pascale.perret univ-grenoble-alpes.fr (pascale[dot]perret[at]univ-grenoble-alpes[dot]fr)
univ-grenoble-alpes.fr (pascale[dot]perret[at]univ-grenoble-alpes[dot]fr)
Tél +33 (0)4 76 63 71 02
et
Alexis Broisat
alexis.broisat inserm.fr (alexis[dot]broisat[at]inserm[dot]fr)
inserm.fr (alexis[dot]broisat[at]inserm[dot]fr)
Senescence :
Jakub Toczek
jakub.toczek inserm.fr (jakub[dot]toczek[at]inserm[dot]fr)
inserm.fr (jakub[dot]toczek[at]inserm[dot]fr)
- Imprimer
- Partager
- Partager sur Facebook
- Partager sur LinkedIn